Caracterización de nuevos genes implicados en metástasis en cáncer de próstata
Characterization of new genes involved in prostate cancer metastasis.Bary Bigay Mercedes1
 , Katlin De La Rosa Poueriet1
, Katlin De La Rosa Poueriet1
1. Instituto ChromoMed, Santo Domingo, República Dominicana.
Descargas
Resumen
Introducción: Nuestro trabajo aborda una revisión bibliográfica realizada entre enero de 2019 y septiembre de 2023, se resalta la importancia de los genes BRCA1, BRCA2, AR y PTEN en la patogénesis, pronóstico y tratamiento del cáncer de próstata, especialmente en su forma metastásica resistente a la castración (mCRPC). Los genes BRCA1 y BRCA2 se identifican como marcadores clave para prever la agresividad del cáncer, sugiriendo la necesidad de terapias dirigidas y vigilancia estricta. La adaptabilidad de las células cancerosas y la variabilidad en la expresión del receptor de andrógenos (AR) limitan la efectividad de las terapias centradas únicamente en AR, señalando la importancia de identificar vías alternativas y biomarcadores para un tratamiento más efectivo. La función de PTEN se relaciona directamente con la progresión de la enfermedad, y su alteración sugiere posibles enfoques terapéuticos. Sin embargo, la heterogeneidad de las células cancerosas y la complejidad de las vías moleculares presentan desafíos significativos para el desarrollo de terapias universales. Conclusión: Los hallazgos promueven la investigación futura para confirmar la aplicabilidad de estos genes como biomarcadores y desarrollar estrategias de tratamiento personalizadas en el cáncer de próstata.
Introducción
El cáncer de próstata es una de las neoplasias más comunes en hombres alrededor del mundo y, aunque en muchos casos es de crecimiento lento y no llega a ser letal, existen formas agresivas de la enfermedad que pueden llevar a la metástasis y, por ende, incrementar significativamente la mortalidad [1]. Entender los mecanismos moleculares y genéticos que subyacen a la progresión y metástasis de este cáncer es crucial para desarrollar tratamientos más efectivos y mejorar el pronóstico para aquellos pacientes afectados.
La metástasis se refiere a la diseminación de células cancerosas desde su lugar de origen a otras partes del cuerpo, donde pueden formar nuevos tumores. Este proceso es complejo y multifacético, e involucra la adquisición de habilidades que permiten a las células del tumor invadir tejidos adyacentes, ingresar al torrente sanguíneo o linfático, sobrevivir en circulación, adherirse y extravasarse en nuevos sitios y, finalmente, proliferar en esos sitios distantes.
Durante las últimas décadas, la investigación en el campo del cáncer de próstata ha identificado varios genes y vías de señalización que están implicados en la progresión tumoral y metástasis. Sin embargo, dada la heterogeneidad y la complejidad del cáncer, es probable que todavía haya muchos genes y mecanismos desconocidos que desempeñen roles fundamentales en estos procesos. La identificación y caracterización de nuevos genes asociados con la metástasis en cáncer de próstata pueden ofrecer perspectivas valiosas sobre la biología del cáncer y, lo más importante, pueden conducir al desarrollo de nuevas terapias dirigidas. Estos genes pueden servir como biomarcadores para la detección temprana, predicción del pronóstico, o como objetivos terapéuticos en sí mismos.
El estudio genómico y transcriptómico, impulsado por las técnicas de secuenciación de nueva generación y herramientas bioinformáticas avanzadas, ha revolucionado nuestra capacidad de descubrir y entender las alteraciones genéticas en cáncer. Utilizando estos enfoques, es posible identificar genes cuya expresión o mutación esté asociada con la metástasis, lo que abre la puerta a intervenciones más precisas y personalizadas.
La importancia de entender la epidemiología del cáncer de próstata (PCa) no puede ser subestimada, dado que es uno de los tipos de cáncer más prevalentes a nivel global y es responsable de un gran número de fallecimientos asociados a esta enfermedad. Dicha comprensión es crucial para desarrollar estrategias efectivas tanto de prevención primaria como secundaria.
Dentro de los factores de riesgo que no pueden ser alterados se encuentran elementos como la edad avanzada, las mutaciones genéticas heredadas, la raza y los antecedentes familiares. Por otro lado, existen también factores de riesgo modificables, tales como el síndrome metabólico, la obesidad y el consumo de tabaco, aunque la evidencia para estos últimos es menos sólida.
Aunque también se han propuesto diversos factores de riesgo relacionados con el estilo de vida, la dieta, el entorno y las infecciones, la solidez de las pruebas que los respaldan es generalmente baja. Con este panorama en mente, esta revisión sistemática y actualizada tiene como objetivo ofrecer una visión integral y actual de la epidemiología del PCa. Esto incluye tanto los factores de riesgo que se pueden modificar como los que no, además de ofrecer recomendaciones para el cribado y estrategias para su optimización.
FACTORES DE RIESGO
Factores de riesgo no modificables
Es notable que el factor de edad tiene un papel significativo en el desarrollo del cáncer de próstata (PCa), tal como lo demuestran diversas estadísticas y estudios. En Estados Unidos, las recientes cifras sobre el cáncer muestran una clara correlación entre la edad avanzada y la incidencia de PCa. Por ejemplo, mientras que la probabilidad de enfrentar un diagnóstico de PCa es del 1.8% para hombres entre 60 y 69 años, este porcentaje se eleva hasta un 9.0% para aquellos que tienen 70 años o más. A lo largo de la vida, la probabilidad acumulada es del 12.5%.
Estudios basados en autopsias añaden otra capa de complejidad a esta relación entre edad y PCa. Según los datos, el 40% de los hombres que superan los 60 años y que no se han sometido a pruebas de detección tienen PCa. Esta cifra aumenta hasta un 60% en el caso de hombres que tienen más de 80 años. Además, es relevante señalar que, según la Sociedad Internacional de Patología Urológica, el 32% de estos cánceres diagnosticados post-mortem son de grado 2 o superior [2].
Historial familiar
Resulta complejo determinar la conexión precisa entre un historial familiar de cáncer de próstata (PCa) y la probabilidad de desarrollar esta enfermedad, aunque está claro que hay un riesgo elevado. Este riesgo no solo se refiere al desarrollo de PCa en general, sino que podría también aplicarse a formas más severas y mortales de la enfermedad. Varios elementos entran en juego al evaluar este riesgo, como el número de familiares afectados, el nivel de parentesco con estos (ya sean familiares de primer o segundo grado), y factores adicionales como su edad al momento del diagnóstico y del fallecimiento debido a PCa.
Además, factores como el tipo de cáncer que otros familiares puedan haber tenido (como cáncer de mama u ovario) o la presencia de enfermedad de alto grado en la familia, pueden complicar aún más la evaluación del riesgo. Hay variables que pueden distorsionar estos datos, como el sesgo de memoria y el estado de salud general de la familia.
Es relevante mencionar que, según los estudios, los hombres que tienen un hermano o un hijo con PCa enfrentan un riesgo que es aproximadamente 2.5 veces mayor de padecer la enfermedad. Este tipo de información es crucial para entender cómo los factores de riesgo familiares pueden contribuir al desarrollo de PCa [2].
Predisposición genética
La heredabilidad genética en el caso del cáncer de próstata (PCa) es notablemente elevada en comparación con otros tipos de cáncer más comunes. Según investigaciones con gemelos, se estima que la heredabilidad del PCa podría ser de aproximadamente un 58%.
Esta susceptibilidad genética se manifiesta de dos maneras distintas: hay factores genéticos que son poco comunes, pero altamente penetrantes, y otros que son más prevalentes, pero generalmente menos penetrantes. Por ejemplo, las mutaciones en los genes HOXB13 y BRCA2 son las más conocidas por su relación con una susceptibilidad autosómica dominante al PCa. Sin embargo, es importante tener en cuenta que estas mutaciones son relativamente raras en la población general, con una prevalencia estimada de solo alrededor del 0.3% [2].
La ciencia está revelando cada vez más la conexión entre el riesgo de cáncer de próstata (PCa) y mutaciones en diversos genes que tienen roles en la reparación del ADN. Entre estos genes, BRCA1, ATM, CHEK2, NBS1 y los asociados con el síndrome de Lynch (como MLH1, MSH2, MSH6 y PMS2) se destacan como particularmente relevantes. Es importante señalar que estas mutaciones tienen una prevalencia más alta en los casos de PCa en etapas avanzadas, especialmente en su forma metastásica, en comparación con el PCa localizado.
En un estudio significativo del UK Biobank que involucró a más de 21,000 hombres, se descubrió que el 1.4% tenía una mutación patogénica rara en al menos uno de los genes clave: BRCA2, HOXB13 y CHEK2. Aunque estas mutaciones son infrecuentes en la población en general y en pacientes con PCa de bajo riesgo, su prevalencia aumenta notablemente en los casos de PCa avanzado, llegando a cifras entre el 10% y el 20%. La variabilidad en la incidencia y agresividad de la enfermedad debido a estas mutaciones genéticas muestra la complejidad de la relación genética y el riesgo de desarrollar PCa.
Estos hallazgos apuntan a la necesidad de seguir investigando para entender completamente cómo estos factores genéticos contribuyen al desarrollo y progresión del PCa [2].
En la búsqueda de entender la correlación entre la calvicie de patrón masculino y el cáncer de próstata (PCa), se han llevado a cabo cuatro metaanálisis significativos. Curiosamente, estos estudios no lograron encontrar un vínculo directo entre la calvicie de patrón masculino en su conjunto y una mayor probabilidad de desarrollar PCa. No obstante, los análisis de subgrupos dentro de estos estudios sí arrojaron hallazgos más específicos.
Concretamente, identificaron una relación entre la calvicie en la región del vértice, que es la parte superior de la cabeza, y un riesgo elevado de padecer PCa.
Este descubrimiento sugiere que, aunque la calvicie de patrón masculino en general no parece estar asociada con un mayor riesgo de PCa, ciertos patrones de calvicie, como la que ocurre en la zona del vértice, podrían ser indicativos de un riesgo aumentado.
Se ha observado que la estatura elevada está correlacionada de forma constante con una probabilidad aumentada de desarrollar cáncer de próstata (PCa), y más específicamente, sus variantes de alto grado. Uno de los mecanismos posibles que podrían explicar esta asociación es la presencia de niveles elevados del factor de crecimiento similar a la insulina durante la etapa de la pubertad.
Este hallazgo sugiere que las dimensiones corporales, en particular la estatura, podrían ser un indicador importante en la evaluación del riesgo de PCa. La relación entre la altura y los niveles de ciertos factores de crecimiento durante etapas críticas del desarrollo podría ofrecer pistas valiosas para entender mejor la etiología de esta enfermedad [2].
Factores de riesgo modificables
Aunque la relación entre el sedentarismo y el aumento del riesgo de cáncer de próstata (PCa) no ha sido claramente establecida por varios estudios, sí se ha observado que un mayor nivel de actividad física puede tener beneficios notables. En particular, las personas más activas físicamente presentan una menor mortalidad específica por PCa y, en el caso de los pacientes ya diagnosticados, mayores tasas de supervivencia libre de la enfermedad. Este efecto positivo se ha observado tanto en actividades físicas intensas como en caminatas a ritmo acelerado. La mayor parte de la investigación en este área se ha centrado en la actividad física recreativa, dejando un vacío en el conocimiento sobre los efectos potenciales de la actividad física en el entorno laboral. Sin embargo, hay indicios que sugieren que mantenerse activo en el trabajo podría también reducir el riesgo de PCa.
Por otro lado, respecto al sueño, su duración no parece tener un efecto significativo en el riesgo general de desarrollar PCa. No obstante, algunos estudios han apuntado a que la calidad del sueño podría estar relacionada con un mayor riesgo de formas agresivas de la enfermedad. Estos hallazgos sugieren que, más allá de la duración del sueño, la calidad de este podría tener un impacto en la severidad del PCa [2].
Entre las diferentes dietas evaluadas por su impacto en el cáncer de próstata (PCa), algunos patrones alimenticios muestran ciertas promesas. La dieta mediterránea, por ejemplo, ha mostrado una asociación protectora modesta contra el PCa en personas que siguen la dieta de manera estricta, aunque otros estudios no respaldan esta relación. Las dietas vegetarianas también muestran potencial, ya que los estudios han confirmado un menor riesgo de PCa en vegetarianos en comparación con los consumidores de carne.
En el ámbito de las dietas basadas en plantas, los hallazgos son mixtos: algunos estudios han encontrado una ligera protección contra el PCa, mientras que otros no han establecido ninguna relación significativa. Sin embargo, se incluyen en este grupo tanto dietas vegetarianas como pesco-vegetarianas y semi-vegetarianas. Cabe destacar que, en estudios de intervención con dietas completamente basadas en plantas, se observaron resultados oncológicos positivos a corto plazo en hombres ya diagnosticados con PCa [2].
En el contexto del cáncer de próstata (PCa), la inflamación dietética parece jugar un papel clave. Varios estudios han investigado la correlación entre una dieta con alto Índice Dietético Inflamatorio y el riesgo de PCa, hallando una asociación positiva en todos los casos. Esta evidencia sugiere que una dieta que fomenta la inflamación podría ser un factor de riesgo para el desarrollo de la enfermedad. Además, la combinación de una dieta que provoca tanto inflamación como hiperinsulinemia podría tener implicaciones aún más serias. Este tipo de dieta se ha relacionado con un incremento en el riesgo de desarrollar formas más agresivas de PCa. Esto subraya la importancia de considerar la naturaleza inflamatoria e hiperinsulinémica de la dieta cuando se evalúan los factores de riesgo para esta forma de cáncer [2].
La relación entre la ingesta de proteínas y el riesgo de cáncer de próstata (PCa) parece ser más compleja de lo que se pensaba inicialmente. Mientras que no se halló una asociación directa entre el consumo total de proteínas y el riesgo de PCa, los datos sugieren que no todas las proteínas son iguales en este contexto.
En particular, la proteína láctea muestra un efecto dosis-dependiente en el riesgo de desarrollar PCa. Para aquellos hombres que consumen más de 30 gramos al día de proteína láctea, el riesgo de PCa aumenta. Cada incremento adicional de 20 gramos al día en la proteína láctea se asocia con un riesgo relativo acumulativo de 1.1%. Este hallazgo destaca la importancia de considerar el tipo de proteínas consumidas, más allá de simplemente la cantidad total, al evaluar factores de riesgo para PCa [2].
La relación entre la exposición ocupacional a ciertas sustancias y el riesgo de cáncer de próstata (PCa) ha sido objeto de varios estudios, pero los resultados son mixtos y no concluyentes. Dos revisiones y metanálisis sobre la exposición al asbesto mostraron resultados dispares: uno no encontró ninguna asociación con el riesgo de PCa, mientras que el otro informó una asociación débil.
También, se estudiaron otros factores laborales, incluida la exposición a compuestos químicos persistentes, bioacumulativos y tóxicos, al insecticida de amplio espectro permetrina, y al estrés laboral. Ninguno de estos factores mostró una correlación con el aumento en el riesgo de PCa. Sin embargo, se identificó una posible asociación positiva con la exposición laboral al cobalto y al cromo hexavalente.
Se observó una mayor probabilidad de desarrollar cáncer de próstata en dos grupos ocupacionales específicos: los bomberos y los trabajadores de la policía. Sin embargo, es importante señalar que los resultados fueron heterogéneos entre los diferentes estudios considerados, y es posible que una mayor tasa de pruebas de PSA en estas poblaciones haya influido en los resultados obtenidos.
Además, se encontró que los trabajadores con exposiciones químicas y a pesticidas en el entorno laboral, como los trabajadores agrícolas y petroleros, enfrentaron un riesgo elevado de cáncer de próstata. Sin embargo, en relación con el esfuerzo físico ocupacional, no se identificó una asociación clara con un mayor riesgo de PCa.
Prevención primaria / quimio prevención
Los inhibidores de la 5-alfa reductasa han sido estudiados en ensayos aleatorizados de alta calidad para evaluar su efecto en el riesgo de cáncer de próstata. Estudios completos han investigado si estos medicamentos pueden reducir el riesgo de cáncer de próstata. Los resultados indican que después de varios años, los hombres que tomaron estos medicamentos tenían menos probabilidad de desarrollar cáncer de próstata en comparación con aquellos que recibieron un placebo inactivo. Esto sugiere que los inhibidores de la 5-alfa reductasa podrían tener un papel importante en la prevención de esta enfermedad [2].
Antiinflamatorios.
El uso regular y continuo de aspirina se ha vinculado con un riesgo menor de desarrollar cáncer de próstata (PCa). Estudios han demostrado que el uso constante de aspirina redujo de manera significativa el riesgo de PCa [2].
Estatinas. El efecto del uso de estatinas en la aparición de cáncer de próstata (PCa) aún es tema de debate, pero la evidencia indica que las estatinas podrían disminuir el riesgo de PCa agresivo y, entre los pacientes diagnosticados, reducir la tasa de mortalidad [2].
Vitaminas y suplementos
Se ha confirmado que la vitamina D no afecta la incidencia general de cáncer de próstata (PCa). No obstante, se observó que niveles más elevados de 25-hidroxivitamina D en la circulación sanguínea están relacionados con un incremento en el riesgo de PCa, presentando una respuesta de dosis no lineal [2].
Prevención secundaria (cribado y detección temprana)
En diciembre de 2022, el Consejo de la Unión Europea recomendó a los países miembros que consideren la posibilidad de establecer programas organizados de detección de cáncer de próstata, empleando pruebas de antígeno prostático específico (PSA) y estudios de resonancia magnética (MRI) [3].
Las directrices emitidas en 2021 por la EAU-EANM-ESTRO-ESUR-SIOG también respaldan la idea de proporcionar pruebas de antígeno prostático específico (PSA) a hombres que estén debidamente informados. Sin embargo, estas directrices sugieren considerar la evaluación y posible interrupción de las pruebas en base a la esperanza de vida y el estado de salud general de los individuos [4].
En los Estados Unidos, las pautas emitidas en 2018 por la Fuerza de Tarea de Servicios Preventivos establecen que los hombres de 55 a 69 años deben tomar decisiones personalizadas acerca de someterse a exámenes periódicos de detección basados en el antígeno prostático específico (PSA) para el cáncer de próstata [5].
El estudio PROMIS demostró que la implementación de resonancia magnética multiparamétrica (mpMRI) previa a la biopsia podría reducir el número de biopsias iniciales en un 27% y llevar a un 5% menos de detecciones de cánceres clínicamente insignificantes en comparación con la biopsia transrectal de ultrasonido (TRUS) estándar. Por su parte, el estudio PRECISION respalda la utilidad de la mpMRI, dado que el 28% de los hombres en el grupo de MRI presentaron una resonancia magnética normal y pudieron evitar la necesidad de someterse a la biopsia [6].
Las mutaciones genéticas son elementos clave en el desarrollo del cáncer, siendo esta enfermedad considerada de origen genético. Estas mutaciones pueden dividirse en dos categorías principales: las mutaciones inactivadoras, que afectan a los genes supresores de tumores, y las mutaciones activadoras, que impactan en los oncogenes.
En el caso de las mutaciones inactivadoras, estas ocurren debido a reorganizaciones estructurales en el genoma, lo que puede resultar en la pérdida de segmentos de ADN a través de deleciones, ya sean extensas o focalizadas. Estos cambios pueden afectar a una o ambas copias de un gen, generando mutaciones monoalélicas o bialélicas.
Por otro lado, las mutaciones activadoras pueden originarse a través de distintos mecanismos, como la amplificación del número de copias de un gen, mutaciones puntuales que afectan a bases individuales del ADN, o reorganizaciones estructurales que llevan a la fusión de genes.
En el contexto del cáncer de próstata, aunque la complejidad de su cariotipo ha complicado su estudio, en la década de 1980 se identificaron alteraciones cromosómicas significativas mediante estudios citogenéticos. Estas alteraciones involucran regiones específicas, como 8p, 8q (locus C-MYC), 10p (locus PTEN), 17q (locus TP53) y el receptor de andrógenos (AR). Los avances tecnológicos, como los marcadores de longitud de fragmentos polimórficos y la hibridación in situ con fluorescencia (FISH), han permitido un análisis más detallado de las alteraciones cromosómicas recurrentes en el cáncer de próstata.
Los avances en tecnologías de alto rendimiento, como la secuenciación de próxima generación (NGS), han brindado una perspectiva extraordinaria sobre el genoma/transcriptoma del PCa. En estudios genómicos recientes basados en NGS, se ha confirmado en su mayoría la presencia de muchos de los eventos genómicos conocidos en el PCa, como la pérdida de PTEN, la mutación/pérdida de TP53. Una observación importante es que algunos eventos como la mutación de SPOP se presenta como la mutación puntual más común en el PCa primario [7].
La presencia o ausencia de fusiones génicas recurrentes entre el gen regulado por andrógenos TMPRSS2 y miembros de la familia ETS (más comúnmente ERG). El perfil completo de número de copias, secuenciación del exoma completo (WES) y secuenciación del genoma completo (WGS) han permitido identificar algunos genes mutados somáticamente con alta recurrencia incluyendo SPOP, TP53, PTEN y FOXA1. Estas evaluaciones computacionales, realizadas en una amplia colección de muestras de prostatectomías caracterizadas mediante WES o WGS, han profundizado nuestra comprensión de los eventos tempranos frente a los eventos posteriores en la carcinogénesis de la próstata [7]. La revolución genómica ha cambiado fundamentalmente nuestra comprensión del cáncer de próstata, desplazando la conversación desde una perspectiva generalizada hacia una mucho más personalizada y precisa.
La identificación de marcadores genéticos, como el BRCA2, especialmente en poblaciones de alto riesgo como hombres con enfermedad metastásica, ha proporcionado una lente a través de la cual se pueden diseñar estrategias de tratamiento más efectivas y precisas. Esta revolución genómica ha sido el impulso detrás de nuevas directrices para llevar a cabo pruebas de ADN germinal en pacientes con cáncer de próstata. No sólo proporciona una imagen más completa del panorama genético del individuo, sino que también abre la puerta a tratamientos dirigidos que son cada vez más específicos y efectivos.
A medida que se revelan más genes asociados al riesgo de cáncer de próstata, se abre un nuevo mundo de posibilidades terapéuticas. Ya estamos viendo cómo la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) ha comenzado a aprobar medicamentos específicos basados en estas identificaciones genéticas. Estos avances representan un gran paso hacia la medicina de precisión en el tratamiento del cáncer de próstata, permitiendo una estrategia más afinada y efectiva que puede variar significativamente de un paciente a otro.
Esta era de medicina genómica no sólo es prometedora para el tratamiento, sino que también tiene implicaciones significativas para la detección temprana y la prevención.
Al entender mejor los factores genéticos que contribuyen al cáncer de próstata, podríamos estar mucho más equipados para realizar intervenciones preventivas eficaces. En un futuro cercano, el acceso a la información genómica podría convertirse en una herramienta estándar en la lucha contra esta enfermedad, cambiando para siempre la forma en que la abordamos.
En esta investigación, nos centraremos en descubrir y entender los “Nuevos genes” que contribuyen al fenómeno de la metástasis en el cáncer de próstata, sin embargo, debido a la que las evidencias de ciertos genes son limitadas, vamos a centrar nuestra caracterización en aquellos genes, que tienen relevancia científica y validez clínica para su uso como biomarcadores genéticos moleculares en el estudio de la progresión a metástasis en el Cáncer de Próstata.
La finalidad de esta revisión bibliográfica es identificar nuevos genes asociados que podrían emplearse para el diagnóstico, seguimiento y tratamiento de esta forma agresiva de cáncer, tales como los citados a continuación:
BRCA1/BRCA2: Aunque más conocidos por su relación con el cáncer de mama y de ovario, estos genes también han sido implicados en el cáncer de próstata avanzado.
PTEN: Este gen es un supresor tumoral y su pérdida o mutación se ha asociado con varios tipos de cáncer, incluido el cáncer de próstata.
AR (Receptor de Andrógenos): Aunque no es un "nuevo" gen, las mutaciones y variantes en este gen siguen siendo un área de investigación intensa, especialmente en relación con la resistencia a la terapia antiandrogénica.
MATERIAL Y MÉTODOS
La metodología no se centró en experimentos de laboratorio ni en la recopilación de datos primarios, sino en la recopilación, análisis y síntesis de literatura previamente publicada sobre el tema.
Selección de muestras
Fuentes. Realizamos una búsqueda exhaustiva en bases de datos y motores de búsquedas académicas y científicas, como PubMed, Scopus, Web of Science, y Google Scholar.
Utilizamos las palabras clave y combinaciones relacionadas con el tema, tales como: "cáncer de próstata", "metástasis", "genes", "caracterización genética", entre otras.
Selección de estudios
Tras obtener un conjunto inicial de estudios, procedimos a la revisión de títulos y resúmenes para seleccionar aquellos que cumplan con los criterios de inclusión. Posteriormente, leer los estudios completos para asegurarse de su relevancia y calidad.
Extracción de datos
Creamos un formato o plantilla para la extracción de datos que contenía: autor(es), año de publicación, título del estudio, genes identificados, tipo de genes y relevancia en la metástasis. Extrajimos la información relevante de cada estudio seleccionado y llenamos la plantilla.
TÉCNICAS DE ANÁLISIS
Análisis y síntesis de la información
Agrupamos los estudios según la fecha de publicación desde los más antiguos hasta los más recientes, genes identificados y resultados del estudio resultados. Realizamos una síntesis de la información recopilada, identificando patrones, coincidencias, diferencias, y gaps en la literatura.
Métodos de validación
En el contexto de una revisión bibliográfica, la validación consistió en asegurarnos de que el estudio sea riguroso y que los resultados sean fiables y reproducibles.
Validación de Fuentes
Utilizamos solo fuentes académicas confiables y revisadas por pares para asegurarnos de que la información que utilizamos es válida y fiable.
Verificación Cruzada de Información
Aseguráramos de que los hallazgos se repiten en múltiples estudios diferentes es una forma de validación.
CRITERIOS DE INCLUSIÓN Y EXCLUSIÓN
Inclusión. Estudios publicados desde el mes de enero del 2019 hasta el mes de septiembre del 2023, artículos de revistas científicas revisadas por pares, estudios que aborden la genética molecular del cáncer de próstata y metástasis, estudios en humanos o tumores humanos, y artículos en inglés.
Exclusión. Estudios anteriores a este período, estudios no revisados por pares, investigaciones no centradas en la genética molecular o que no se refieran al cáncer de próstata, estudios en animales y artículos en idiomas distintos al inglés.
RESULTADOS Y DISCUSIÓN
Genes BRCA1 y BRCA2
Se han revisado 464 estudios, publicados en PubMed, Scopus, Web of Science, y Google Scholar, desde enero del año 2019 hasta septiembre del año 2023, relacionados con el cáncer de próstata, de los cuales solo 12 cumplieron los criterios de inclusión, los mismos abordan la relación entre la genética y el cáncer de próstata, organizados en orden cronológico desde los más recientes hasta los más antiguos. Estos estudios han investigado la presencia de mutaciones en genes supresores de tumores, como BRCA1 y BRCA2, y su influencia en el riesgo, agresividad y pronóstico del cáncer de próstata.
Los estudios más recientes, realizados en 2023, han destacado la importancia de la genética en la estratificación del riesgo y el desarrollo de terapias dirigidas en el cáncer de próstata. Se ha observado que las mutaciones en BRCA2 se asocian con enfermedad más agresiva y alta mortalidad específica por cáncer de próstata.
Además, se ha encontrado una mayor frecuencia de mutaciones en genes supresores de tumores como BRCA2 en pacientes con cáncer de próstata. Estos estudios han subrayado la necesidad de considerar la genética en la identificación temprana de pacientes de alto riesgo y en la toma de decisiones terapéuticas.
El estudio de Oh M et al. (2019) y el de Tommy Nyberg et al. (2020) ofrecen una línea base sólida para entender cómo las mutaciones en BRCA1/2 están asociadas con un mayor riesgo y mortalidad. Específicamente, Nyberg y colegas enfatizan que la ubicación de la mutación dentro del gen y los antecedentes familiares también son factores cruciales. Esto sugiere que no todas las mutaciones BRCA2 son iguales y que el contexto genético y familiar podría ser crucial para interpretar el riesgo.
Hussain M et al. (2020) van más allá y examinan la eficacia del medicamento Olaparib en un subconjunto de pacientes con alteraciones en BRCA1/2. Este estudio sugiere un camino para intervenciones terapéuticas personalizadas basadas en el perfil genético del paciente, respaldando la importancia de la detección genética temprana para guiar la terapia.
Junejo NN et al. (2020) y Patel VL et al. (2020) establecen un vínculo claro entre las mutaciones BRCA2 y una progresión más rápida de la enfermedad, incluido un tiempo de supervivencia más corto y grados más altos en la escala Gleason.
El estudio de Dall'Era MA et al. (2020) expande el enfoque más allá de BRCA1/2, incluyendo otros genes de reparación del ADN como ATM, MSH6, y MSH2. El hallazgo de que aproximadamente un 16% de una cohorte de 944 hombres tenía al menos una mutación en estos genes sugiere que la atención no debe limitarse solo a BRCA1/2.
Wokolorczyk D et al. (2020) ofrecen una perspectiva geográfica, sugiriendo que la prevalencia de mutaciones y su relación con la agresividad del cáncer de próstata pueden variar según la población, lo que indica la necesidad de estudios más diversificados a nivel mundial.
Stadler ZK et al. (2021) y Valsecchi AA et al. (2023) señalan la importancia de ampliar la terapia dirigida y abordan las limitaciones actuales de la aplicación clínica de estos hallazgos genéticos. En particular, Valsecchi señala que las mutaciones somáticas son más comunes que las de línea germinal, un área que requiere más investigación.
Estos estudios demuestran que las mutaciones en BRCA1/2 y otros genes relacionados con la reparación del ADN juegan un papel significativo en la agresividad y el pronóstico del cáncer de próstata. Sin embargo, las implicaciones clínicas de estos hallazgos, como la implementación de terapias personalizadas y la detección temprana, aún están en desarrollo. Además, futuras investigaciones podrían centrarse en el impacto de las mutaciones somáticas frente a las germinales, así como en la variabilidad geográfica y étnica en estos patrones de mutación.
Gen AR (Receptor de Andrógenos)
En el corpus de 159 artículos revisados en PubMed, Scopus, Web of Science, y Google Scholar, que se centraron en el receptor de andrógenos (AR), solo 10 cumplieron con los estrictos criterios de inclusión, lo que subraya la complejidad y los desafíos en la investigación de cáncer de próstata metastásico resistente a la castración (mCRPC).
Estos 10 estudios son particularmente importantes ya que ofrecen hallazgos clínicos y moleculares robustos, centrados específicamente en cómo AR y sus vías asociadas impactan en la progresión y tratamiento de la metástasis en mCRPC.
Uno de los puntos clave es la adaptabilidad de las células cancerosas. Los estudios indican que, incluso cuando se inhibe AR, las células cancerosas pueden adaptarse y encontrar vías alternativas para sobrevivir y metastatizar. Esto plantea un desafío significativo en la gestión clínica de mCRPC, sugiriendo que las terapias dirigidas solo a AR podrían no ser suficientemente efectivas para prevenir o controlar la metástasis.
En cuanto a las implicaciones para la metástasis, la plasticidad de las células cancerosas en mCRPC es especialmente preocupante. Los estudios muestran una tendencia hacia la heterogeneidad en la expresión de AR durante el tratamiento, así como un aumento en la expresión de marcadores neuroendocrinos. Esto podría permitir que las células cancerosas colonicen nuevos tejidos más fácilmente, haciendo que la enfermedad sea más difícil de tratar y más probable que se disemine.
Además, las alteraciones en AR y en otros genes como TP53, RB1, y PTEN tienen implicaciones directas en cómo y dónde ocurre la metástasis. Estas mutaciones genéticas podrían servir como biomarcadores para predecir qué pacientes tienen mayor riesgo de desarrollar metástasis y podrían beneficiarse de tratamientos más agresivos o de nuevas modalidades terapéuticas. Estos estudios aportan un valioso conocimiento sobre el papel que desempeña AR en la metástasis de mCRPC, y subrayan la necesidad de estrategias terapéuticas más complejas y personalizadas.
Al reconocer la adaptabilidad y la heterogeneidad de las células cancerosas en mCRPC, así como las diversas mutaciones y vías que contribuyen a la metástasis, los investigadores y los médicos pueden acercarse más a la personalización del tratamiento para mejorar los resultados en esta enfermedad complicada y devastadora.
Gen PTEN
Después de revisar 414 artículos científicos en PubMed, Scopus, Web of Science, y Google Scholar, asociados al gen PTEN en relación con el cáncer de próstata, sólo 13 cumplieron con los criterios de inclusión para un análisis detallado. Específicamente, el enfoque de este análisis está en los hallazgos relacionados con la metástasis, un fenómeno crítico que complica notablemente el tratamiento y el pronóstico del cáncer de próstata.
Los artículos demuestran que la pérdida de función o la mutación del gen PTEN está estrechamente relacionada con la progresión hacia estados avanzados y metastásicos del cáncer. Por ejemplo, un estudio del 2020 titulado "Genomics of lethal prostate cancer at diagnosis and castration resistance" señala que la pérdida de función en genes como TP53, RB1 y PTEN es más común en casos de cáncer de próstata metastásico resistente a la castración (mCRPC) en comparación con estados no metastásicos del cáncer. Este hallazgo sugiere un rol crítico de PTEN en la agresividad y la resistencia al tratamiento del cáncer avanzado.
Otro artículo del 2022, "Prevalencia y pronóstico de dianas terapéuticas de próxima generación en el cáncer de próstata metastásico resistente a la castración", amplía este entendimiento al vincular la pérdida de PTEN con una supervivencia libre de progresión más corta en pacientes tratados con abiraterona, un fármaco comúnmente utilizado en mCRPC. Este estudio sugiere que las alteraciones en PTEN podrían usarse como un biomarcador para predecir la respuesta al tratamiento y, potencialmente, como una diana terapéutica.
Es claro que PTEN juega un papel clave no solo en la iniciación del cáncer de próstata, sino también en su progresión hacia estados metastásicos. Estos hallazgos plantean la posibilidad de que el restablecimiento de la función normal de PTEN, o la modulación de sus vías de señalización, puedan ofrecer estrategias terapéuticas novedosas en el tratamiento del cáncer de próstata metastásico. La heterogeneidad tumoral y la complejidad de las vías de señalización implicadas en la metástasis hacen que el desarrollo de terapias efectivas sea un desafío.En definitiva, los artículos seleccionados ofrecen evidencia robusta de la importancia del gen PTEN en la metástasis del cáncer de próstata, abriendo nuevas avenidas para el desarrollo de estrategias terapéuticas dirigidas y un tratamiento más efectivo.
CONCLUSIONES
Nuestra revisión bibliográfica sobre el cáncer de próstata realizada con artículos científicos extraídos de PubMed, Scopus, Web of Science y Google Scholar, entre el periodo de enero del año 2019 a septiembre del año 2023 ha destacado la importancia crítica de varios genes involucrados en la patogénesis, el pronóstico y el tratamiento de esta enfermedad, particularmente en su forma metastásica resistente a la castración (mCRPC).
Genes BRCA1 y BRCA2
Estos genes son marcadores claves en la identificación de pacientes que tienen un riesgo más alto de desarrollar formas más agresivas del cáncer de próstata.
La presencia de mutaciones en BRCA1 y BRCA2 podría abrir puertas a terapias dirigidas específicas, además de una vigilancia más estricta.
Los estudios subrayan que más investigaciones son necesarias para entender el papel exacto que juegan estos genes en el cáncer de próstata y cómo pueden integrarse de manera efectiva en las estrategias de tratamiento.
Gen AR (Receptor de Andrógenos)
Las células cancerosas tienen la capacidad de adaptarse y encontrar vías alternativas para sobrevivir, lo que hace que las terapias centradas solo en el AR sean insuficientes.
Los estudios han mostrado una variabilidad en la expresión del AR durante el tratamiento, y un aumento en la expresión de marcadores neuroendocrinos, que hacen más difícil el control de la enfermedad.
Las mutaciones en AR y en genes como TP53, RB1, y PTEN podrían usarse para predecir el comportamiento de la enfermedad y ser objetivos para futuras terapias.
Gen PTEN
Papel en la Progresión de la Enfermedad: Se observa una estrecha relación entre la pérdida de función o mutaciones en PTEN y la progresión hacia estados más avanzados y metastásicos del cáncer de próstata.
Los cambios en PTEN pueden influir en la efectividad de tratamientos existentes como la abiraterona y podrían usarse para guiar decisiones terapéuticas.
Los estudios sugieren que el restablecimiento de la función de PTEN o la modulación de sus vías de señalización podrían ofrecer estrategias de tratamiento novedosas.
La adaptabilidad y la heterogeneidad de las células cancerosas, sumadas a la complejidad de las vías moleculares implicadas, dificultan la creación de terapias universalmente efectivas.
Los resultados son preliminares y se necesita más investigación para confirmar estos hallazgos, especialmente para entender cómo se pueden implementar de manera efectiva como biomarcadores clínicos y en que etapa de la enfermedad. La adaptabilidad y la heterogeneidad de las células cancerosas, junto con la complejidad de las vías moleculares implicadas, representan desafíos significativos para el desarrollo de terapias efectivas.
Aunque estos hallazgos ofrecen direcciones prometedoras para el tratamiento personalizado del cáncer de próstata y la utilización de los genes caracterizados a los fines de ser usados como biomarcadores, es necesario llevar a cabo más investigaciones para validar estos resultados y comprender completamente sus aplicaciones clínicas.
TABLAS


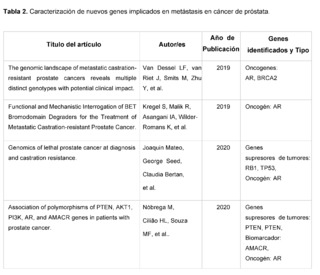

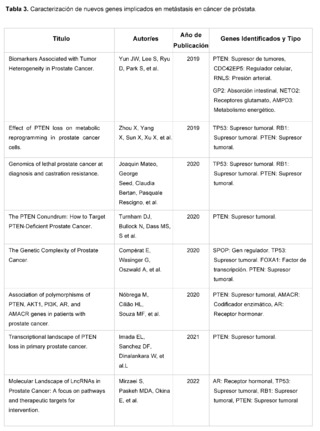
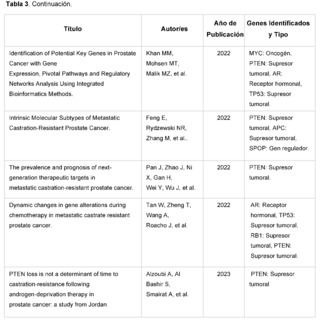
Citas
[1] Organización Panamericana de la Salud. (2020). Cáncer. Recuperado de https://www.paho.org/es/temas/cancer
[2] Bergengren, O., Pekala, K. R., Matsoukas, K., Fainberg, J., Mungovan, S. F., Bratt, O., Bray, F., Brawley, O., Luckenbaugh, A. N., Mucci, L., Morgan, T. M. y Carlsson, S. V. (2023). Actualización 2022 sobre la epidemiología y factores de riesgo del cáncer de próstata: Una revisión sistemática. European Urology, 84(2), 191-206.
[3] Consejo de la Unión Europea. (2022, 9 de diciembre). El Consejo actualiza su Recomendación para el cribado del cáncer [Comunicado de prensa]. https://data.consilium.europa.eu/doc/document/ST-14770-2022-INIT/es/pdf
[4] Mottet, N., van den Bergh, R. C. N., Briers, E., Van den Broeck, T., Cumberbatch, M. G., De Santis, M., ... & Cornford, P. (2021). EAU-EANM-ESTRO-ESUR-SIOG Guidelines on Prostate Cancer-2020 Update. Part 1: Screening, Diagnosis, and Local Treatment with Curative Intent. European Urology, 79(2), 243-262. https://doi.org/10.1016/j.eururo.2020.09.042
[5] Plambeck, B. D., Wang, L. L., McGirr, S., Jiang, J., Van Leeuwen, B. J., LaGrange, C. A., & Boyle, S. L. (2022). Effects of the 2012 and 2018 US Preventive Services Task Force prostate cancer screening guidelines on pathologic outcomes after prostatectomy. Prostate, 82(2), 216-220. doi: 10.1002/pros.24261.
[6] El-Shater Bosaily, A., Parker, C., Brown, L. C., Gabe, R., Hindley, R. G., Kaplan, R., ... Ahmed, H. U. (2015). PROMIS—Prostate MR imaging study: A paired validating cohort study evaluating the role of multi-parametric MRI in men with clinical suspicion of prostate cancer. Contemporary Clinical Trials, 42, 26-40. https://doi.org/10.1016/j.cct.2015.02.008
[7] Rubin, M. A., & Demichelis, F. (2019). The Genomics of Prostate Cancer: A Historic Perspective. Cold Spring Harbor Perspectives in Medicine, 9(3), a034942. https://doi.org/10.1101/cshperspect.a034942
[8] Oh, M., Alkhushaym, N., Fallatah, S., Althagafi, A., Aljadeed, R., Alsowaida, Y., Jeter, J., Martin, J. R., Babiker, H. M., McBride, A., & Abraham, I. (2019). The association of BRCA1 and BRCA2 mutations with prostate cancer risk, frequency, and mortality: A meta-analysis. Prostate, 79(8), 880-895. https://doi.org/10.1002/pros.23795
[9] Nyberg, T., Frost, D., Barrowdale, D., Evans, D. G., Bancroft, E., Adlard, J., Ahmed, M., Barwell, J., Brady, A. F., Brewer, C., Cook, J., Davidson, R., Donaldson, A., Eason, J., Gregory, H., Henderson, A., Izatt, L., Kennedy, M. J., Miller, C., Morrison, P. J., Murray, A., Ong, K. R., Porteous, M., Pottinger, C., Rogers, M. T., Side, L., Snape, K., Walker, L., Tischkowitz, M., Eeles, R., Easton, D. F., & Antoniou, A. C. (2020). Prostate Cancer Risks for Male BRCA1 and BRCA2 Mutation Carriers: A Prospective Cohort Study. European Urology, 77(1), 24-35. https://doi.org/10.1016/j.eururo.2019.08.025
[10] Hussain, M., Mateo, J., Fizazi, K., Saad, F., Shore, N., Sandhu, S., Chi, K. N., Sartor, O., Agarwal, N., Olmos, D., Thiery-Vuillemin, A., Twardowski, P., Roubaud, G., Özgüroğlu, M., Kang, J., Burgents, J., Gresty, C., Corcoran, C., Adelman, C. A., & de Bono, J.; PROfound Trial Investigators. (2020). Survival with Olaparib in Metastatic Castration-Resistant Prostate Cancer. The New England Journal of Medicine, 383(24), 2345-2357. https://doi.org/10.1056/NEJMoa2022485
[11] Junejo, N. N., & AlKhateeb, S. S. (2020). BRCA2 gene mutation and prostate cancer risk: Comprehensive review and update. Saudi Medical Journal, 41(1), 9-17. https://doi.org/10.15537/smj.2020.1.24759
[12] Patel, V. L., Busch, E. L., Friebel, T. M., Cronin, A., Leslie, G., McGuffog, L., ... & Rebbeck, T. R. (2020). Association of Genomic Domains in BRCA1 and BRCA2 with Prostate Cancer Risk and Aggressiveness. Cancer Research, 80(3), 624-638. https://doi.org/10.1158/0008-5472.CAN-19-1840
[13] Dall'Era, M. A., McPherson, J. D., Gao, A. C., DeVere White, R. W., Gregg, J. P., & Lara, P. N. Jr. (2020). Germline and somatic DNA repair gene alterations in prostate cancer. Cancer, 126(13), 2980-2985. https://doi.org/10.1002/cncr.32908
[14] Wokołorczyk, D., Kluźniak, W., Huzarski, T., Gronwald, J., Szymiczek, A., Rusak, B., Stempa, K., Gliniewicz, K., Kashyap, A., Morawska, S., Dębniak, T., Jakubowska, A., Szwiec, M., Domagała, P., Lubiński, J., Narod, S. A., Akbari, M. R., Cybulski, C., & the Polish Hereditary Prostate Cancer Consortium. (2020). Mutations in ATM, NBN and BRCA2 predispose to aggressive prostate cancer in Poland. International Journal of Cancer, 147(10), 2793-2800. https://doi.org/10.1002/ijc.33272
[15] Stadler, Z. K., Maio, A., Chakravarty, D., Kemel, Y., Sheehan, M., Salo-Mullen, E., Tkachuk, K., Fong, C. J., Nguyen, B., Erakky, A., Cadoo, K., Liu, Y., Carlo, M. I., Latham, A., Zhang, H., Kundra, R., Smith, S., Galle, J., Aghajanian, C., Abu-Rustum, N., Varghese, A., O'Reilly, E. M., Morris, M., Abida, W., Walsh, M., Drilon, A., Jayakumaran, G., Zehir, A., Ladanyi, M., Ceyhan-Birsoy, O., Solit, D. B., Schultz, N., Berger, M. F., Mandelker, D., Diaz, L. A. Jr., Offit, K., & Robson, M. E. (2021). Therapeutic Implications of Germline Testing in Patients With Advanced Cancers. Journal of Clinical Oncology, 39(24), 2698-2709. https://doi.org/10.1200/JCO.20.03661
[16] McNevin, C. S., Cadoo, K., Baird, A. M., Murchan, P., Sheils, O., McDermott, R., & Finn, S. (2021). Pathogenic BRCA Variants as Biomarkers for Risk in Prostate Cancer. Cancers (Basel), 13(22), 5697. https://doi.org/10.3390/cancers13225697
[17] Nguyen-Dumont, T., Dowty, J. G., MacInnis, R. J., Steen, J. A., Riaz, M., Dugué, P. A., Renault, A. L., Hammet, F., Mahmoodi, M., Theys, D., Tsimiklis, H., Severi, G., Bolton, D., Lacaze, P., Sebra, R., Schadt, E., McNeil, J., Giles, G. G., Milne, R. L., & Southey, M. C. (2021). Rare Germline Pathogenic Variants Identified by Multigene Panel Testing and the Risk of Aggressive Prostate Cancer. Cancers (Basel), 13(7), 1495. https://doi.org/10.3390/cancers13071495
[18] Rajwa, P., Quhal, F., Pradere, B., Gandaglia, G., Ploussard, G., Leapman, M. S., Gore, J. L., Paradysz, A., Tilki, D., Merseburger, A. S., Morgan, T. M., Briganti, A., Palapattu, G. S., & Shariat, S. F. (2023). Prostate cancer risk, screening and management in patients with germline BRCA1/2 mutations. Nature Reviews Urology, 20(4), 205-216. https://doi.org/10.1038/s41585-022-00680-4
[19] Valsecchi, A. A., Dionisio, R., Panepinto, O., Paparo, J., Palicelli, A., Vignani, F., & Di Maio, M. (2023). Frequency of Germline and Somatic BRCA1 and BRCA2 Mutations in Prostate Cancer: An Updated Systematic Review and Meta-Analysis. Cancers (Basel), 15(9), 2435. https://doi.org/10.3390/cancers15092435
[20] Van Dessel, L. F., van Riet, J., Smits, M., Zhu, Y., Hamberg, P., van der Heijden, M. S., Bergman, A. M., van Oort, I. M., de Wit, R., Voest, E. E., Steeghs, N., Yamaguchi, T. N., Livingstone, J., Boutros, P. C., Martens, J. W. M., Sleijfer, S., Cuppen, E., Zwart, W., van de Werken, H. J. G., Mehra, N., & Lolkema, M. P. (2019). The genomic landscape of metastatic castration-resistant prostate cancers reveals multiple distinct genotypes with potential clinical impact. Nature Communications, 10(1), 5251. https://doi.org/10.1038/s41467-019-13084-7
[21] Kregel, S., Malik, R., Asangani, I. A., Wilder-Romans, K., Rajendiran, T., Xiao, L., Vo, J. N., Soni, T., Cieslik, M., Fernadez-Salas, E., Zhou, B., Cao, X., Speers, C., Wang, S., & Chinnaiyan, A. M. (2019). Functional and Mechanistic Interrogation of BET Bromodomain Degraders for the Treatment of Metastatic Castration-resistant Prostate Cancer. Clinical Cancer Research, 25(13), 4038-4048. https://doi.org/10.1158/1078-0432.CCR-18-3776
[22] Mateo, J., Seed, G., Bertan, C., Rescigno, P., Dolling, D., Figueiredo, I., Miranda, S., Nava Rodrigues, D., Gurel, B., Clarke, M., Atkin, M., Chandler, R., Messina, C., Sumanasuriya, S., Bianchini, D., Barrero, M., Petermolo, A., Zafeiriou, Z., Fontes, M., Perez-Lopez, R., Tunariu, N., Fulton, B., Jones, R., McGovern, U., Ralph, C., Varughese, M., Parikh, O., Jain, S., Elliott, T., Sandhu, S., Porta, N., Hall, E., Yuan, W., Carreira, S., & de Bono, J. S. (2020). Genomics of lethal prostate cancer at diagnosis and castration resistance. Journal of Clinical Investigation, 130(4), 1743-1751. https://doi.org/10.1172/JCI132031
[23] Nóbrega, M., Cilião, H. L., Souza, M. F., Souza, M. R., Serpeloni, J. M., Fuganti, P. E., & Cólus, I. M. S. (2020). Association of polymorphisms of PTEN, AKT1, PI3K, AR, and AMACR genes in patients with prostate cancer. Genetics and Molecular Biology, 43(3), e20180329. https://doi.org/10.1590/1678-4685-GMB-2018-0329
[24] Li, Y., Yang, R., Henzler, C. M., Ho, Y., Passow, C., Auch, B., Carreira, S., Nava Rodrigues, D., Bertan, C., Hwang, T. H., Quigley, D. A., Dang, H. X., Morrissey, C., Fraser, M., Plymate, S. R., Maher, C. A., Feng, F. Y., de Bono, J. S., & Dehm, S. M. (2020). Diverse AR Gene Rearrangements Mediate Resistance to Androgen Receptor Inhibitors in Metastatic Prostate Cancer. Clinical Cancer Research, 26(8), 1965–1976. https://doi.org/10.1158/1078-0432.CCR-19-3023
[25] Lin, Y. W., Wen, Y. C., Chu, C. Y., Tung, M. C., Yang, Y. C., Hua, K. T., Pan, K. F., Hsiao, M., Lee, W. J., & Chien, M. H. (2020). Stabilization of ADAM9 by N-α-acetyltransferase 10 protein contributes to promoting progression of androgen-independent prostate cancer. Cell Death & Disease, 11(7), 591. https://doi.org/10.1038/s41419-020-02786-2
[26] Das, R., Sjöström, M., Shrestha, R., Yogodzinski, C., Egusa, E. A., Chesner, L. N., Chen, W. S., Chou, J., Dang, D. K., Swinderman, J. T., Ge, A., Hua, J. T., Kabir, S., Quigley, D. A., Small, E. J., Ashworth, A., Feng, F. Y., & Gilbert, L. A. (2021). An integrated functional and clinical genomics approach reveals genes driving aggressive metastatic prostate cancer. Nature Communications, 12(1), 4601. https://doi.org/10.1038/s41467-021-24919-7
[27] Zhang, X., Huang, Z., Wang, J., Ma, Z., Yang, J., Corey, E., Evans, C. P., Yu, A. M., & Chen, H. W. (2021). Targeting Feedforward Loops Formed by Nuclear Receptor RORγ and Kinase PBK in mCRPC with Hyperactive AR Signaling. Cancers (Basel), 13(7), 1672. https://doi.org/10.3390/cancers13071672
[28] Tan, W., Zheng, T., Wang, A., Roacho, J., Thao, S., Du, P., Jia, S., Yu, J., King, B. L., & Kohli, M. (2022). Dynamic changes in gene alterations during chemotherapy in metastatic castrate resistant prostate cancer. Scientific Reports, 12(1), 4672. https://doi.org/10.1038/s41598-022-08520-6
[29] Sandhu, H. S., Portman, K. L., Zhou, X., Zhao, J., Rialdi, A., Sfakianos, J. P., Guccione, E., Kyprianou, N., Zhang, B., & Mulholland, D. J. (2022). Dynamic plasticity of prostate cancer intermediate cells during androgen receptor-targeted therapy. Cell Reports, 40(4), 111123. https://doi.org/10.1016/j.celrep.2022.111123
[30] Yun, J. W., Lee, S., Ryu, D., Park, S., Park, W. Y., Joung, J. G., & Jeong, J. (2019). Biomarkers Associated with Tumor Heterogeneity in Prostate Cancer. Translational Oncology, 12(1), 43-48. https://doi.org/10.1016/j.tranon.2018.09.003
[31] Zhou, X., Yang, X., Sun, X., Xu, X., Li, X., Guo, Y., Wang, J., Li, X., Yao, L., Wang, H., & Shen, L. (2019). Effect of PTEN loss on metabolic reprogramming in prostate cancer cells. Oncology Letters, 17(3), 2856-2866. https://doi.org/10.3892/ol.2019.9932
[32] Mateo, J., Seed, G., Bertan, C., Rescigno, P., Dolling, D., Figueiredo, I., Miranda, S., Nava Rodrigues, D., Gurel, B., Clarke, M., Atkin, M., Chandler, R., Messina, C., Sumanasuriya, S., Bianchini, D., Barrero, M., Petermolo, A., Zafeiriou, Z., Fontes, M., Perez-Lopez, R., Tunariu, N., Fulton, B., Jones, R., McGovern, U., Ralph, C., Varughese, M., Parikh, O., Jain, S., Elliott, T., Sandhu, S., Porta, N., Hall, E., Yuan, W., Carreira, S., & de Bono, J. S. (2020). Genomics of lethal prostate cancer at diagnosis and castration resistance. Journal of Clinical Investigation, 130(4), 1743-1751. https://doi.org/10.1172/JCI132031
[33] Turnham, D. J., Bullock, N., Dass, M. S., Staffurth, J. N., & Pearson, H. B. (2020). The PTEN Conundrum: How to Target PTEN-Deficient Prostate Cancer. Cells, 9(11), 2342. https://doi.org/10.3390/cells9112342
[34] Compérat, E., Wasinger, G., Oszwald, A., Kain, R., Cancel-Tassin, G., & Cussenot, O. (2020). The Genetic Complexity of Prostate Cancer. Genes (Basel), 11(12), 1396. https://doi.org/10.3390/genes11121396
[35] Nóbrega, M., Cilião, H. L., Souza, M. F., Souza, M. R., Serpeloni, J. M., Fuganti, P. E., & Cólus, I. M. S. (2020). Association of polymorphisms of PTEN, AKT1, PI3K, AR, and AMACR genes in patients with prostate cancer. Genetic and Molecular Biology, 43(3), e20180329. https://doi.org/10.1590/1678-4685-GMB-2018-0329
[36] Imada, E. L., Sanchez, D. F., Dinalankara, W., Vidotto, T., Ebot, E. M., Tyekucheva, S., Franco, G. R., Mucci, L. A., Loda, M., Schaeffer, E. M., Lotan, T., & Marchionni, L. (2021). Transcriptional landscape of PTEN loss in primary prostate cancer. BMC Cancer, 21(1), 856. https://doi.org/10.1186/s12885-021-08593-y
[37] Mirzaei, S., Paskeh, M. D. A., Okina, E., Gholami, M. H., Hushmandi, K., Hashemi, M., Kalu, A., Zarrabi, A., Nabavi, N., Rabiee, N., Sharifi, E., Karimi-Maleh, H., Ashrafizadeh, M., Kumar, A. P., & Wang, Y. (2022). Molecular Landscape of LncRNAs in Prostate Cancer: A focus on pathways and therapeutic targets for intervention. Journal of Experimental & Clinical Cancer Research, 41(1), 214. https://doi.org/10.1186/s13046-022-02406-1
[38] Khan, M. M., Mohsen, M. T., Malik, M. Z., Bagabir, S. A., Alkhanani, M. F., Haque, S., Serajuddin, M., & Bharadwaj, M. (2022). Identification of Potential Key Genes in Prostate Cancer with Gene Expression, Pivotal Pathways and Regulatory Networks Analysis Using Integrated Bioinformatics Methods. Genes (Basel), 13(4), 655. https://doi.org/10.3390/genes13040655
[39] Feng, E., Rydzewski, N. R., Zhang, M., Lundberg, A., Bootsma, M., Helzer, K. T., Lang, J. M., Aggarwal, R., Small, E. J., Quigley, D. A., Sjöström, M., & Zhao, S. G. (2022). Intrinsic Molecular Subtypes of Metastatic Castration-Resistant Prostate Cancer. Clinical Cancer Research, 28(24), 5396-5404. https://doi.org/10.1158/1078-0432.CCR-22-2567
[40] Pan, J., Zhao, J., Ni, X., Gan, H., Wei, Y., Wu, J., Zhang, T., Wang, Q., Freedland, S. J., Wang, B., Song, S., Ye, D., Liu, C., & Zhu, Y. (2022). The prevalence and prognosis of next-generation therapeutic targets in metastatic castration-resistant prostate cancer. Molecular Oncology, 16(22), 4011-4022. https://doi.org/10.1002/1878-0261.13320
[41] Tan, W., Zheng, T., Wang, A., Roacho, J., Thao, S., Du, P., Jia, S., Yu, J., King, B. L., & Kohli, M. (2022). Dynamic changes in gene alterations during chemotherapy in metastatic castrate resistant prostate cancer. Scientific Reports, 12(1), 4672. https://doi.org/10.1038/s41598-022-08520-6
[42] Alzoubi, A., Al Bashir, S., Smairat, A., Alrawashdeh, A., Haddad, H., & Kheirallah, K. (2023). PTEN loss is not a determinant of time to castration-resistance following androgen-deprivation therapy in prostate cancer: A study from Jordan. Journal of Medical Life, 16(4), 593-598. https://doi.org/10.25122/jml-2023-0034

